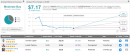
För 11 månader sedan, USA Food and Drug Administration (FDA) stängde Solid Biosciences (SLDB) "IGNITE DMD" fas I/II klinisk prövning efter att en av de unga patienterna som var involverade i prövningen drabbats av en "allvarlig biverkning". Trots att patienten i fråga återhämtat sig, inga nya patienter drabbats av sådana allvarliga biverkningar, och företaget förser FDA med "information och åtgärder avsedda att förbättra patientsäkerheten" och "data relaterade till förbättringar av tillverkningsprocessen", avböjde FDA att tillåta försök med återupptas i juli och bad Solid Biosciences att ge ännu mer information om sina försök och om de säkerhetsåtgärder som man föreslog att lägga till för att få försöken på rätt spår igen. Spola framåt tre månader till och — framgång! På torsdagen bekräftade Solid Biosciences att FDA har "lyft det kliniska hållet" på sina prövningar, och erkänner att företaget har "tillfredsställande åtgärdat alla frågor om kliniska stopp." Framöver planerar företaget att ta bort de flesta tomma virala kapsider (proteinskalet som innehåller viralt material) och begränsa den maximala vikten av barnpatienter som går in i sina försök till 18 kilo, för att minska virusmängden av SGT-001 terapi som patienterna utsätts för. Som namnet antyder syftar Solid Biosciences IGNITE DMD-studier till att bromsa eller vända effekterna av Duchennes muskeldystrofi (DMD), en genetisk sjukdom som orsakar progressiv muskeldegeneration och svaghet främst hos unga pojkar från två år och uppåt (vilket förklarar den låga maximal vikt för försöksdeltagare). Företagets SGT-001 är en genterapi som injicerar ett modifierat virus i en patient, innehållande DNA kodat för att åtgärda problemen som orsakar sjukdomen. Åtminstone är detta vad som borde hända i teorin. IGNITE DMD-prövningarna är utformade för att ta reda på om det fungerar i praktiken, och tack vare FDA:s omprövning kommer nu dessa prövningar att tillåtas att återupptas - förmodligen under det första kvartalet 2021. I en notis på torsdag bekräftade Chardan-analytikern Gbola Amusa att FDA:s beslut sätter utvecklingen av SGT-001 "på kurs" mot en global marknadsmöjlighet på 50 miljarder USD. Om den godkänns kommer behandlingen att vara en av endast "relativt få" genterapier som någonsin har godkänts för mänsklig användning globalt, vilket ger Solid Biosciences en ledande position på denna marknad. Och eftersom genterapiprodukter som SGT-001 anses vara "nya, komplexa och relativt svåra att tillverka", skulle hindren för inträde på denna marknad för konkurrenter vara betydande. Analytikern ser detta som en "stor möjlighet" - en inte utan risker, men en som kan, om behandlingen visar sig, lyfta Solid Biosciences-aktien från sitt nuvarande pris på $4 och ändras hela vägen till $12.50 eller mer. Detta nya prismål är förresten mer än dubbelt så mycket som Amusa värderade företaget till innan FDA:s beslut i torsdags, och innebär 208% uppsida från nuvarande nivåer. Och faktiskt, Amusa funderar på att "med framsteg" kan behandlingen "ta SLDB avsevärt över vårt uppdaterade kursmål på $12.50" - och noterar upprepade gånger att Solid Biosciences-aktien till och med nått "topnivåer på > $50/sh, ” vilket antyder att den eventuella uppsidan kan bli ännu större än vad han är beredd att postulera idag. (För att se Amusas meritlista, klicka här) Sammantaget har SLDB ett Moderate Buy-betyg från analytikerkonsensus, baserat på 2 "köp" och 1 "håll"-betyg. Aktierna säljs för 4.06 USD och det genomsnittliga kursmålet på 7.17 USD innebär en uppåtpotential på 79 %. (Se SLDB-aktieanalys på TipRanks)För att hitta bra idéer för vårdaktier som handlas till attraktiva värderingar, besök TipRanks' Best Stocks to Buy, ett nyligen lanserat verktyg som förenar alla TipRanks aktieinsikter. Friskrivningsklausul: De åsikter som uttrycks i den här artikeln är endast de av de presenterade analytikerna. Innehållet är endast avsett att användas i informationssyfte.
,
